Una
reacción química es un proceso termodinámico en el cual dos o más sustancias
denominadas reactantes (elementos o compuestos) se combinan y se transforman de
manera tal que ocurre un cambio en sus estructuras moleculares y enlaces para
luego formar otras sustancias llamadas productos.
Este
fenómeno también es conocido como cambio químico ya que a diferencia de las
mezclas, no solo ocurre una combinación entre varias sustancias y un cambio
físico, sino que también acontece un cambio interno y estructural de cada una
de ellas.
Cuando
sucede una reacción química esta generalmente viene acompañada de ciertas
características que nos permitirá clasificarla o identificarla, como por
ejemplo, cambio de olor, variación de la temperatura, variación de color,
formación de un precipitado o desprendimiento de gases, entre otros.
De
igual manera, para que se lleve a cabo ciertas reacciones, en algunos casos, se
necesita de intermediarios para que estas ocurran, por ejemplo la temperatura y
el uso de catalizadores.
Reacciones
endotérmicas
Se entiende por reacciones endotérmicas a
cierto tipo de reacciones químicas (o sea: el proceso de transformación de dos
o más sustancias en otras diferentes) que al ocurrir consumen energía calórica,
es decir, en las cuales los productos obtenidos poseen mayores niveles
energéticos que los reactivos iniciales, ya que han tomado parte del calor del
ambiente.
Esto se resume en la
formulación siguiente: dada una entalpía (H), una reacción endotérmica siempre
tendrá una variación de entalpía (ΔH) mayor a cero (ΔH>0). Recordemos además
que la entalpía es la variable que representa el intercambio de energía entre
un sistema termodinámico y su entorno.
Este tipo de reacciones
son de uso común en la industria del hielo químico y del enfriamiento, ya que
pueden suscitarse en ambientes controlados para retirar calor de los ambientes
o de otras sustancias. Posteriormente, algunas de dichas aplicaciones fueron
reemplazadas con el frío generado por electricidad (compresores).
Algunos
ejemplos de reacción endotérmica son:
·
La producción de Ozono en la
atmósfera. Impulsada por la radiación ultravioleta del sol, los
átomos de oxígeno (O2) son convertidos en ozono (O3), absorbiendo energía de
dicha radiación en el proceso.
·
La hidrólisis del agua. Para
separar el hidrógeno (H) y el oxígeno (O) que componen el agua (H2O), es
necesario añadir energía eléctrica en
un procedimiento conocido como hidrólisis, en el cual ambos tipos de átomos
responden a los polos generados por la corriente eléctrica añadida, rompiéndose
su unión molecular (y consumiendo energía).
·
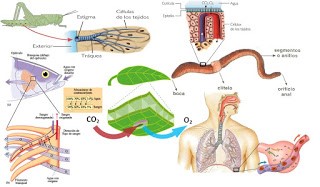
La fotosíntesis. El proceso
de nutrición de las plantas se da a través de una serie de reacciones químicas
que descomponen el dióxido de carbono (CO2) ambiental,
en presencia de agua y, necesariamente, de luz solar. Esto se debe a que dicha
reacción requiere de un añadido de energía a consumirse durante la reacción. (Enciclopedia de conceptos, 2018)
Se entiende por una
reacción exotérmica (del griego –exo, “hacia afuera”, y thermos, “calor”)
aquellas reacciones químicas que al producirse liberan o desprenden energía, ya
sea en forma de calor, luz u otras formas de energía. Son en ese sentido
contrarias a las reacciones endotérmicas, que absorben energía.
Toda
reacción exotérmica se caracteriza por que los niveles de energía de sus
reactivos son mayores que los de su producto, lo cual significa que parte de la
energía química contenida en sus enlaces se ha liberado bajo una nueva forma.
Estas reacciones son de suma importancia para la bioquímica, por ejemplo, ya
que son ellas justamente las que un organismo viviente propicia en su
metabolismo para obtener energía.
La
mayoría de las reacciones exotérmicas son de oxidación, y de ser muy violentas
pueden generar fuego, tal y como la combustión. Lo mismo ocurre en las
transiciones de la materia de un estado de agregación a otro de menor energía,
como de gas a líquido (condensación), por ejemplo, o de líquido a sólido
(solidificación).
De
hecho, muchas reacciones exotérmicas son peligrosas para la salud porque la
energía liberada es abrupta y sin control, pudiendo producir quemaduras u otros
daños a los seres vivientes.
Algunas reacciones exotérmicas conocidas son:
·
La combustión. Al inyectar un mínimo de energía calórica a un combustible (como
la gasolina, el gas natural, el gas metano, etc.) en presencia de oxígeno, se
produce un fenómeno exotérmico conocido como combustión, y que no es más que
una oxidación violenta, en la cual se produce fuego: luz y calor, que puede
canalizarse para ser una explosión (energía cinética), como ocurre en los
motores de combustión interna.
·
Oxidación de la glucosa. Esta es la reacción que llevamos a cabo los animales para obtener
energía metabólica: tomamos el oxígeno de la respiración y lo usamos para
oxidar los azúcares, rompiendo la molécula de glucosa en moléculas más simples
(glucólisis) y obteniendo como recompensa moléculas de ATP, ricas en energía química.
·
Mezcla de potasio y agua. El potasio es un potente desecante (base fuerte) que al ser
mezclado con agua libera hidrógeno y enormes cantidades de energía en una
explosión. Esto ocurre con todos los metales alcalinos o alcalinotérreos,
aunque no siempre con la misma cantidad de energía liberada.
La formación de amoníaco. Para formar el
amoníaco (NH3) se hace reaccionar nitrógeno (N2) e hidrógeno (H2), lo cual
supone la obtención de una molécula menos energética que las moléculas puestas
en reacción. Esa diferencia de energía debe liberarse, y ocurre como un
incremento de temperatura (calor). (Enciclopedia de conceptos, 2018)
Véase también en:
https://concepto.de/reacciones-endotermicas/#ixzz5aE5Fi9rm
https://concepto.de/reaccion-exotermica/#ixzz5aE6KYJqO
https://concepto.de/reaccion-exotermica/#ixzz5aE6KYJqO


No hay comentarios.:
Publicar un comentario